هي أساساً ما يصف خاصيات وسلوك انتقال الحرارة وإنتاج الشغل سواء كان شغلا كهربائيا أو من خلال عمليات ثروموديناميكية، منذ وضع هذه القوانين أصبحت قوانين معتمدة ضمن قوانين الفيزياء والعلوم الفيزيائية
140- قوانين #الديناميكا_الحرارية | الجزء الأول
--------
هي أساسا ما يصف خاصيات وسلوك انتقال الحرارة وإنتاج الشغل سواء كان شغلا كهربائيا أو من خلال عمليات ثروموديناميكية، منذ وضع هذه القوانين أصبحت قوانين معتمدة ضمن قوانين الفيزياء والعلوم الفيزيائية (كيمياء، علم المواد، علم الفلك ...)
- القانون الصفري:
يصف القانون الصفري التوازن الحراري بين الأجسام المتلامسة أو في نظام حراري وينشأ القانون عن تعريف درجة الحرارة.
درجة حرارة الجسم هي مؤشر على كمية الطاقة المختزنة داخل الجسم كما أنها مؤشرعلى مدى حركية ذراته.
- القانون الأول للديناميكيا الحرارية:
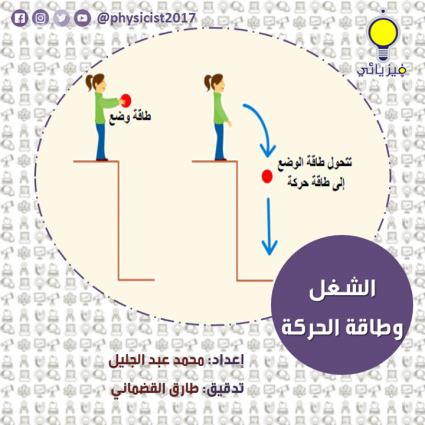
هو تعبير لمبدأ حفظ الطاقة، أي أن الطاقة تتغير من حالة إلى أخرى ومن طاقة كامة إلى طاقة نشطة.
وبتعبير آخر: إن الطاقة لا تفنى ولا تستحدث من العدم، وإنما تتحول من صورة إلى أخرى. ويشخص القانون أن نقل الحرارة بين الأنظمة كنوع من أنواع الطاقة.
إن ارتفاع الطاقة الداخلية لنظام ثرموديناميكي معين يساوي كمية الطاقة الحرارية المضافة للنظام، مطروح منه الشغل الميكانيكي المبذول من النظام إلى الوسط المحيط.
- القانون الأول للديناميكا الحرارية للنظام المغلق:
dQ=dU+dW
(dQ) هي كمية الحرارة التي تخرج من أو تنتقل إلى النظام
(dU) هو التغير في الطاقة الداخلية للنظام وهي هنا دالة لدرجة الحرارة فقط
(dW)هو الشغل المبذول على أو من النظام فإذا كان النظام غازا فيكون الشغل هو حاصل ضرب الضغط p في تغيرالحجم dV
dW=P.dV
والوحدة القياسية هي الجول.
- القانون الأول للديناميكا الحرارية للنظام المفتوح:
dQ-dW=dH+dKin+dPot
حيث أن : dQ كمية الحرارة المضافة أو المنزوعة من النظام.
dW الشغل المبذول من النظام أو عليه
dH التغير في المحتوى الحراري
dKin التغير في طاقة الحركة
dPot التغير في طاقة الوضع
في حالة الحجم الثابت:
v ثابت هذا يعنى أن dv=0وبالتالي لا شغل يؤدي إلى dW=0
وهذا يعني أن كمية الحرارة التي يمتصها النظام تتناسب مع الزيادة في درجة الحرارة.
وتكون : dU=dH
أي يكون التغير في المحتوى الحراري مساويا للتغير في الطاقة الداخلية.
في حالة درجة الحرارة الثابتة:
تكون dT=0
وهذا يعنى أن dU=0
وفي هذه الحالة تكون dH=dW
أي أن كمية الحرارة التي يمتصها النظام تساوي الشغل المبذول بواسطة الغاز.
إعداد: جيجي يوسف.
تدقيق: زكرياء لوطفي.
#فيزيائي
#الفيزياء_للجميع


 أديان
أديان علوم
علوم منوع
منوع ثقافة
ثقافة أدبيات
أدبيات تاريخ وجغرافيا
تاريخ وجغرافيا تقني
تقني